╗»īWĄõą═īŹ“×┐éĮY
ę╗Īó┐šÜŌųąč§ÜŌ║¼┴┐Ą─£yČ©
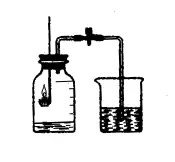
1.▓┘ū„▓Į¾EŻ║į┌╝»ÜŌŲ┐ā╚╝ė╚ļ╔┘┴┐╦«Ż¼▓óīó╦«├µ╔ŽĘĮ┐šķgĘų×ķ5Ą╚Ę▌ĪŻė├ų╣╦«ŖA╝ėŠo─zŲż╣▄ĪŻ³c╚╝╚╝¤²│ūā╚Ą─╝t┴ū║¾ĪŻ┴ó╝┤╔ņ╚ļŲ┐ųą▓ó░č╚¹ūė╚¹ŠoŻ¼ė^▓ņ╝t┴ū╚╝¤²Ą─¼FŽ¾ĪŻ┤²╝t┴ūŽ©£ń▓ó└õģs║¾Ż¼┤“ķ_ų╣╦«ŖAŻ¼ė^▓ņīŹ“×¼FŽ¾╝░╦«├µĄ─ūā╗»ŪķørĪŻ
2.īŹ“×¼FŽ¾Ż║ėą┤¾┴┐░ū¤¤«a╔·Ż¼╝»ÜŌŲ┐ā╚╦«├µ╔Ž╔²┴╦╝s1/5¾wĘeĪŻ
3.īŹ“×ĮYšōŻ║č§ÜŌ¾wĘe╝sš╝┐šÜŌ¾wĘeĄ─1/5ĪŻ
4.ūóęŌ╩┬ĒŚŻ║ó┘╝t┴ūę¬╚ĪūŃ┴┐╗“▀^┴┐;ó┌īŹ“×Ū░Öz▓ķčbų├ÜŌ├▄ąį;ó█ų╣╦«ŖAŖAŠo;ó▄³c╚╝╝t┴ū║¾┴ó╝┤╔ņ╚ļŲ┐ųą▓ó░č╚¹ūė╚¹Šo;ó▌ę¬└õģs═Ļ╚½ĪŻ
Č■ĪóĖ▀Õi╦ßŌøųŲč§
1.▓┘ū„▓Į¾EŻ║▓ķ-čb-Č©-³c-╩š-ļx-Ž©
2.īŹ“×¼FŽ¾Ż║ėą┤¾┴┐ÜŌ¾w▀M╚ļ╝»ÜŌŲ┐ųąĪŻ
3.īŹ“×ĮYšōŻ║└¹ė├Ė▀Õi╦ßŌø┐╔ęįųŲč§ĪŻ
4.ūóęŌ╩┬ĒŚŻ║
ó┘įć╣▄┐┌┬įŽ“Ž┬āAą▒Ż║Ę└ų╣└õ─²╦«Ą╣┴„ę²Ųįć╣▄ŲŲ┴č
ó┌╦ÄŲĘŲĮõüį┌įć╣▄Ą─Ąū▓┐Ż║Š∙ä“╩▄¤ß
ó█ĶFŖAŖAį┌ļx╣▄┐┌╝s1/3╠Ä
ó▄ī¦╣▄æ¬╔į┬Č│÷ŽŲż╚¹Ż║▒Ńė┌ÜŌ¾w┼┼│÷
ó▌įć╣▄┐┌æ¬Ę┼ę╗łF├▐╗©Ż║Ę└ų╣Ė▀Õi╦ßŌøĘ█─®▀M╚ļī¦╣▄
ó▐┼┼╦«Ę©╩š╝»ĢrŻ¼┤²ÜŌ┼▌Š∙ä“▀B└m├░│÷Ģrį┘╩š╝»(äéķ_╩╝┼┼│÷Ą─╩Ūįć╣▄ųąĄ─┐šÜŌ)
ó▀īŹ“×ĮY╩°ĢrŻ¼Ž╚ęŲī¦╣▄į┘Ž©£ńŠŲŠ½¤¶Ż║Ę└ų╣╦«Ą╣╬³ę²Ųįć╣▄š©┴č
óÓė├Ž“╔Ž┼┼┐šÜŌĘ©╩š╝»ÜŌ¾wĢrŻ¼ī¦╣▄╔ņĄĮ╝»ÜŌŲ┐Ąū▓┐
╚²ĪóļŖĮŌ╦«
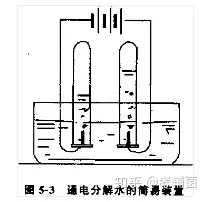
1.▓┘ū„▓Į¾EŻ║į┌ę╗éĆ╩óėą╦«Ą─╦«▓█ųąĄ╣┴óā╔ų¦╩óØM╦«Ą─įć╣▄Ż¼Įė═©
ų▒┴„ļŖį┤Ż¼ė^▓ņļŖśO╔Ž║═įć╣▄ā╚ėą╩▓├┤¼FŽ¾░l╔·ĪŻŪąöÓčbų├Ą─ļŖį┤Ż¼į┌╦«Ž┬ė├─┤ųĖČ┬ūĪįć╣▄┐┌Ż¼░čįć╣▄╚Ī│÷Ż¼ų▒┴ó║¾╦╔ķ_─┤ųĖŻ¼┴ó╝┤░čĦėą╗ąŪĄ──ŠŚl╔ņ╚ļįć╣▄Ż¼▀Mąąė^▓ņĪŻ
2.īŹ“×¼FŽ¾Ż║═©ļŖ║¾Ż¼ļŖśO╔Ž│÷¼F┴╦ÜŌ┼▌Ż¼═©ļŖę╗Č╬Ģrķgęį║¾Ż¼š²Īóžōā╔śO«a╔·Ą─ÜŌ¾w¾wĘe▒╚┤¾╝s×ķ1Ż║2ĪŻ╔ņ╚ļš²śOįć╣▄└’Ą─Ħ╗ąŪ─ŠŚl╚╝¤²Ż¼žōśOįć╣▄└’Ą─ÜŌ¾w/╚╝¤²▓ó│÷¼FĄŁ╦{╔½╗čµĪŻ
3.īŹ“×ĮYšōŻ║╦«╩Ūė╔ÜõĪóč§ā╔ĘNį¬╦žĮM│╔Ą─ĪŻ
4.ūóęŌ╩┬ĒŚŻ║ó┘╦«ųą┐╔╝ė╚ļ╔┘┴┐┴“╦ßŌc╗“Üõč§╗»Ōcęįį÷ÅŖī¦ļŖąįĪŻó┌į┌īŹ“×▀M│╠äéķ_╩╝ĢrŻ¼č§ÜŌ║═ÜõÜŌĄ─¾wĘe▒╚┼c1:2▓╗Ę¹Ż¼╩Ūę“×ķč§ÜŌ▓╗ęū╚▄ė┌╦«Ż¼Ą½Ģ■╚▄ĮŌę╗ąĪ▓┐Ęų;ÜõÜŌļy╚▄Ż¼Ę┤æ¬╦┘┬╩▌^┬²Ż¼╦∙ęįÜõÜŌ▌^╔┘ĪŻ
╦─Īó─Š╠┐▀ĆįŁč§╗»Ń~
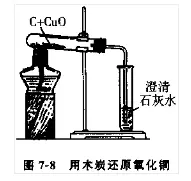
1.▓┘ū„▓Į¾EŻ║░čäé║µĖ╔Ą──Š╠┐Ę█─®║═č§╗»Ń~Ę█─®╗ņä“Ż¼ąĪą─ĄžõüĘ┼▀Mįć╣▄Ż¼▓óīóįć╣▄╣╠Č©į┌ĶF╝▄┼_╔ŽĪŻįć╣▄┐┌čbėą═©╚ļ│╬ŪÕ╩»╗ę╦«Ą─ī¦╣▄Ż¼ė├ŠŲŠ½¤¶╝ė¤ß╗ņ║Ž╬’ÄūĘųńŖĪŻ╚╗║¾Ž╚│Ę│÷ī¦ÜŌ╣▄Ż¼┤²įć╣▄└õģs║¾į┘░čįć╣▄└’Ą─Ę█─®Ą╣į┌╝ł╔ŽŻ¼ė^▓ņ¼FŽ¾ĪŻ
2.īŹ“×¼FŽ¾Ż║║┌╔½Ę█─®ųØuūā×ķ╝t╔½Ż¼╩»╗ę╦«ūā£åØßĪŻ
3.īŹ“×ĮYšōŻ║╠╝Š▀ėą▀ĆįŁąįĪŻ
4.ūóęŌ╩┬ĒŚŻ║ó┘Ę┤æ¬═Ļ║¾Ž╚īó╩óėą╩»╗ę╦«Ą─įć╣▄ęŲū▀Ż¼Ę└ų╣ę║¾wĄ╣╬³▀M╚ļįć╣▄Ż¼╩╣¤ßĄ─įć╣▄š©┴čĪŻó┌īŹ“×═Ļ«ģ▓╗─▄┴ó╝┤īóįć╣▄ā╚Ą─╬’┘|Ą╣│÷ė^▓ņŻ¼Ę└ų╣Ė▀£žĄ─Ń~┼c┐šÜŌųąĄ─č§ÜŌĘ┤æ¬ųžą┬č§╗»│╔č§╗»Ń~ĪŻ
╬ÕĪóę╗č§╗»╠╝▀ĆįŁč§╗»Ń~
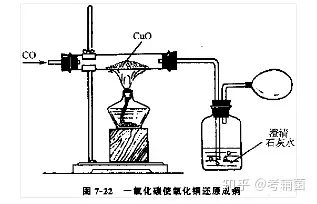
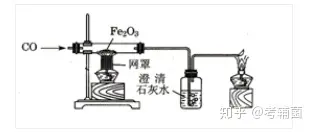
1.▓┘ū„▓Į¾EŻ║░┤╚ńłD╦∙╩ŠĄ─čbų├į┌▓Ż┴¦╣▄└’Ę┼╚ļč§╗»Ń~Ż¼Ž╚═©COŻ¼║¾╝ė¤ßŻ¼Ę┤æ¬═Ļ«ģŽ╚═Żų╣╝ė¤ßŻ¼ų┴▓Ż┴¦╣▄└õģs║¾═Żų╣═©╚ļCOĪŻ
2.īŹ“×¼FŽ¾Ż║║┌╔½╣╠¾wūā│╔╝t╔½Ż¼│╬ŪÕ╩»╗ę╦«ūā£åØ߯¼─®Č╦ī¦╣▄╠Ä«a╔·╦{╔½╗čµĪŻ
3.īŹ“×ĮYšōŻ║ę╗č§╗»╠╝Š▀ėą▀ĆįŁąįĪŻ
4.ūóęŌ╩┬ĒŚŻ║īŹ“×Ū░ę¬ī”ę╗č§╗»╠╝▀Mąą“×╝āĪŻ
┴∙ĪóĶFĄ─ę▒¤Æ
1.▓┘ū„▓Į¾EŻ║░┤╚ńłD╦∙╩ŠĄ─čbų├į┌▓Ż┴¦╣▄└’Ę┼╚ļč§╗»ĶFŻ¼Ž╚═©COŻ¼║¾╝ė¤ßŻ¼Ę┤æ¬═Ļ«ģŽ╚═Żų╣╝ė¤ßŻ¼ų┴▓Ż┴¦╣▄└õģs║¾═Żų╣═©╚ļCOĪŻ
2.īŹ“×¼FŽ¾Ż║▓Ż┴¦╣▄└’Ą─Ę█─®ė╔╝tūž╔½ųØuūā║┌Ż¼│╬ŪÕ╩»╗ę╦«ūā£åØßĪŻ
3.īŹ“×ĮYšōŻ║¤ÆĶFĄ─įŁ└ĒŠ═╩Ū└¹ė├ę╗č§╗»╠╝┼cč§╗»ĶFĄ─Ę┤æ¬ĪŻ
4.ūóęŌ╩┬ĒŚŻ║Ę┤æ¬ĮY╩°║¾æ¬Ž╚═Żų╣╝ė¤ßŻ¼┤²└õģs║¾═Żų╣═©ÜŌĪŻ
Ų▀ĪóĶFųŲŲĘõP╬gŚl╝■
1.▓┘ū„▓Į¾EŻ║
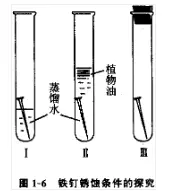
(1)į┌Ą┌ę╗ų¦įć╣▄ųąĘ┼╚ļę╗Ė∙ĶFßöŻ¼ūó╚ļš¶s╦«Ż¼▓╗ę¬Į■ø]ĶFßöŻ¼╩╣ĶFßö┼c┐šÜŌ║═╦«Įėė|ĪŻ
(2)į┌Ą┌Č■ų¦įć╣▄ųąĘ┼╚ļę╗Ė∙ĶFßöŻ¼ūó╚ļäéų¾Ęą▀^Ą─š¶s╦«(ęį┌sū▀╦«ųą╚▄ĮŌĄ─┐šÜŌ)ų┴Į■ø]ĶFßöŻ¼╚╗║¾į┌╦«├µ╔Ž╝ėę╗īėų▓╬’ė═Ż¼╩╣ĶFßöų╗┼c╦«Įėė|ĪŻ
(3)īóĄ┌╚²ų¦įć╣▄ė├ŠŲŠ½¤¶║µĖ╔Ż¼Ę┼╚ļę╗Ė∙ĶFßöŻ¼ė├ŽŲż╚¹╚¹Šoįć╣▄┐┌Ż¼╩╣ĶFßöų╗┼cĖ╔į’Ą─┐šÜŌĮėė|ĪŻ
├┐╠ņė^▓ņĶFßö╔·õPĄ─ŪķørŻ¼▓óšJšµū÷║├ėøõøĪŻ
2.īŹ“×¼FŽ¾Ż║ó±ųąĶFßö╔·õPŻ¼ó“ųąĶFßö▓╗╔·õPŻ¼ó¾ųąĶFßö▓╗╔·õPĪŻ
3.īŹ“×ĮYšōŻ║ĶF╔·õPĄ─▀^│╠īŹļH╔Ž╩ŪĶF┼c┐šÜŌųąĄ─č§ÜŌ║═╦«š¶ÜŌ░l╔·╗»īWĘ┤æ¬Ą─▀^│╠ĪŻ
4.ūóęŌ╩┬ĒŚŻ║ó┘ę¬ė├š¶s╦«;ó┌ę¬ė├ØŹā¶¤oõPĄ─ĶFßöĪŻ
ĪĪĪĪ ÜgėŁ╩╣ė├╩ųÖCĪóŲĮ░ÕĄ╚ęŲäėįOéõįLå¢ųą┐╝ŠWŻ¼2024ųą┐╝ę╗┬Ę┼Ń░ķ═¼ąąŻĪ>>³cō¶▓ķ┐┤















